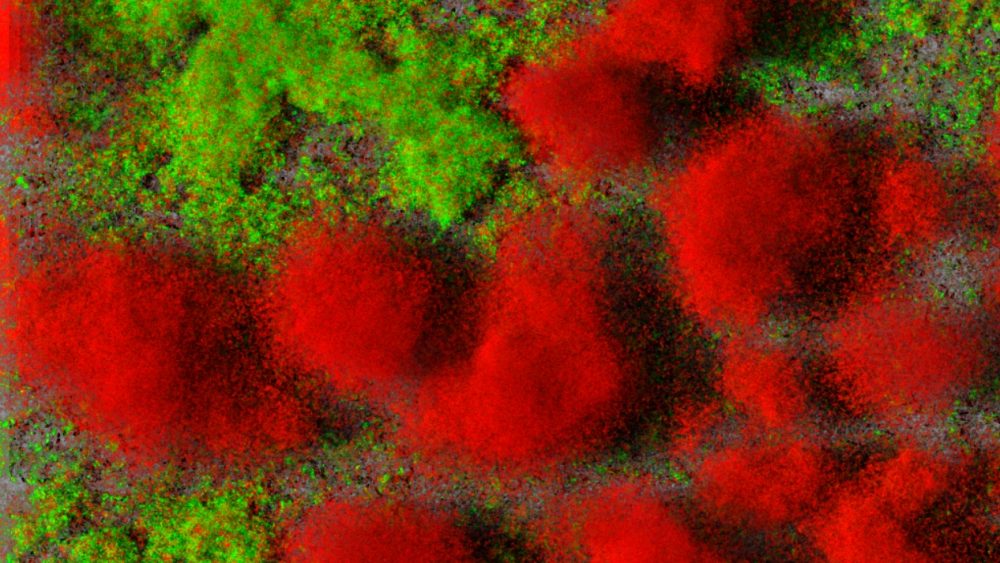
Bakterien in der Matrix
Biofilme und die Suche nach dem Antibiotikum 2.0
Bakterien „erkennen“ Grenzflächen und setzen sich dort dann fest. In diesem Zustand bilden sie mit anderen Bakterien in der Nähe Gemeinschaften. Die Bewohner schützen ihre Kolonie durch die Herausbildung einer dicken Schleimschicht, auch Matrix genannt, und verändern darin sogar ihr Verhalten. Solche Biofilme sind nicht nur Ursache der gefürchteten Krankenhauskeime, sondern können im Körper chronische bakterielle Infektionen hervorrufen, die sich bis heute aufgrund der hohen Widerstandsfähigkeit der Biofilmstruktur mit Antibiotika kaum therapieren lassen. Die Suche nach den zellulären Grundlagen der Verhaltensänderung hat begonnen.
Sprechertext der Sendung:
Wenn der Mikrobiologe von „Biofilmen“ spricht, dann meint er verschiedenste Aggregationen von Bakterien. Sie schließen sich zu komplexen Gemeinschaften zusammen und bilden kollektive Lebensformen, vergleichbar mit Korallenriffen oder Bienenvölkern. Sie leben in einer dicken schleimigen Substanz, die der Experte als Matrix oder EPS bezeichnet.
Kein natürlicher Biofilm gleicht dem anderen. Er ist geprägt vom zufälligen Beisammensein unterschiedlicher Bakterienarten. Das bunte Kollektiv hat dabei erstaunliche Fähigkeiten – dazu gehört auch das Recyceln von organischem Material. Biofilme sind oft unsichtbar, aber überall. Sie fressen auf diesem Planeten alles, was ihnen unter kommt – wählerisch sind sie dabei nicht: von abgestorbenen Pflanzen bis zu Tier-Fäkalien – alles wird als Nahrung genutzt. Diese hochwertige Materialverarbeitung haben sich viele Organismen für ihr Verdauungssystem längst zunutze gemacht. Wiederkäuer ebenso wie der Mensch: sein Mikrobiom im Darm ist nichts anderes als ein hochspezialisierter Biofilm.
Selbst der Ingenieur setzt die erstaunlichen Verwertungs-Fähigkeiten der Mikrostrukturen technologisch ein: beispielsweise bei der biologischen Reinigung von Trink- und Abwasser, wo Biofilme heute genutzt werden, um organische Stoffe abzubauen.
Der inzwischen emeritierte Hans-Curt Flemming ist einer der Pioniere der Disziplin, die er in den siebziger Jahren mit begründet hat. Er baute das erste deutsche Forschungsinstitut auf, das Biofilm Centre an der Uni Duisburg. Seit fast zwanzig Jahren widmet es sich ausschließlich der interdisziplinären Erforschung von Biofilmen. Flemming ist fasziniert von diesem Kollektiv mit den erstaunlichen Fähigkeiten.
Statement – Prof. Dr. Hans-Curt Flemming, Mikrobiologe und Gründer des Biofilm Centre, Emeritus Universität Duisburg-Essen
Trotzdem: Biofilme haben derzeit in der Presse ein ziemlich schlechtes Image. Sie sind in Kliniken allgegenwärtig und dort nur noch schwer zu beherrschen. Selbst Implantate im Körper können sie befallen. Meist gibt es dann nur eine Therapie: deren Austausch. Denn eingebettet in ihrem Schleim, sind die Aggregationen bakterieller Einzeller ausgesprochen widerstandsfähig. Der Mikrobiologe spricht dabei von Toleranzverhalten. Weder Desinfektionsmittel noch Antibiotika können die Bakterien in ihrer Matrix gänzlich vernichten. Die im Inneren gut geschützten Einzeller kannibalisieren die Toten um sie herum und nehmen aus der Umgebung sofort weitere Mitglieder in ihre Wohngemeinschaft auf. So entwickeln sie neue, häufig noch resistentere Aggregationen.
Ursache für ihre erhöhte Widerstandsfähigkeit ist, dass die Einzeller erkennen, ob sie einzeln frei in der Luft schweben oder im Wasser schwimmen – oder aber an eine Oberfläche andocken. Sobald das geschieht, beginnt ihr neues Leben in der Matrix. Im direkten Austausch mit ihren Mitbewohnern ändern sie ihr Verhalten bis hin zur kollektiven Aufgabenteilung.
Statement – Prof. Dr. Hans-Curt Flemming, Mikrobiologe und Gründer des Biofilm Centre, Emeritus Universität Duisburg-Essen
Das bessere Verständnis dieser Toleranz ist der Schlüssel für künftige Therapien, um den menschlichen Organismus besser als bisher gegen Biofilm-assoziierte Infektionen zu schützen. Denn erst in den letzten beiden Jahrzehnten hat sich mehr und mehr die Erkenntnis durchgesetzt: Die schlechte Wirksamkeit von Antibiotika bei solchen Krankheiten entsteht durch das geänderte Verhalten der Einzeller in der Matrix.
Die Mikrobiologin Karin Sauer forscht daran, wie die Struktur dieser Biofilme künftig zerstört werden könnte. Sie sieht drei Behandlungsstrategien, die derzeit im Fokus stehen.
Statement Prof. Dr. Karin Sauer – Mikrobiologin und Co-Direktorin Binghamton Center for Biofilm Research, New York
Wir sind am Helmholtz-Zentrum für Infektionsforschung. Hier befassen sich die Mikrobiologen genau mit dieser Frage: Wie ändern sich die Verhaltensmuster von Bakterien in Biofilmen ? Sie versuchen, die Grundlagen dieser Verhaltensänderungen zu entschlüsseln – um sie später in einer Therapie beeinflussen zu können.
Statement Janne Thöming – Mikrobiologin, Twincore (Joint Venture von Helmholtz-Zentrum für Infektionsforschung und Medizinische Hochschule Hannover)
Die Genexpression ist also ein wichtiges Steuerungselement in der Zelle. Sie legt fest, welches Set an Informationen, die in den Genen der DNA vorliegen, tatsächlich umgesetzt wird. Das wiederum hängt unter anderem vom aktuellen Zustand der Zelle ab – beispielsweise eben davon, ob das Bakterium frei schwimmt, sich gerade auf einer Oberfläche festgesetzt hat oder schon in einem reifen Biofilm lebt. Aber auch Stress und viele andere Faktoren beeinflussen die komplexe Genexpression, mit der dann die Produktion der unterschiedlichen Stoffwechselkomponenten beginnt.
Die Wissenschaftler am Helmholtz-Zentrum für Infektionsforschung untersuchen die Verhaltensweisen von Bakterien in ihren beiden Zustandsformen: konventionell freischwimmend – und fest sitzend in einem Biofilm. Der bioinformatische Vergleich der gewaltigen Datenmengen soll typische Muster in den veränderten Genexpressionen beider Zustände aufdecken.
Statement Janne Thöming – Mikrobiologin, Twincore (Joint Venture von Helmholtz-Zentrum für Infektionsforschung und Medizinische Hochschule Hannover)
Gesucht wird also ein „allgemeiner Toleranz-Mechanismus“, einer, der allen Biofilm-Bakterien zugrunde liegt. Ob es ihn tatsächlich gibt und wie er funktioniert, ist heute eine noch ungeklärte wissenschaftliche Frage.
Statement Janne Thöming – Mikrobiologin, Twincore (Joint Venture von Helmholtz-Zentrum für Infektionsforschung und Medizinische Hochschule Hannover)
Auch wenn wir derzeit die genauen Zusammenhänge noch nicht kennen: Schon jetzt zeichnet sich ab, dass auch die Herausbildung der Matrix in direkter Wechselwirkung der Vorgänge in den Bakterien steht und die Herausbildung des Toleranzverhaltens beeinflusst. Was also passiert, wenn wir nicht die Zelle, sondern direkt den Biofilm attackieren? Das genau ist das Forschungsgebiet von Karin Sauer.
Statement Prof. Dr. Karin Sauer – Mikrobiologin und Co-Direktorin Binghamton Center for Biofilm Research, New York
Die Zerstörung des Schleims und die zelluläre Verhaltensänderung von Bakterien: Das müssen für die Zukunft keine alternativen therapeutischen Ansätze sein.
Statement Prof. Dr. Karin Sauer – Mikrobiologin und Co-Direktorin Binghamton Center for Biofilm Research, New York
Doch bei allen ersten Erfolgen der Biofilm-Bekämpfung im Labor gilt auch: Bis zur Entwicklung von hochwirksamen Medikamenten mit einem Antibiotikum 2.0 ist es noch ein langer Weg. Denn das, was heute in der Petrischale schon gut klappt, muss noch lange nicht im Organismus funktionieren.
Statement – Prof. Dr. Hans-Curt Flemming, Mikrobiologe und Gründer des Biofilm Centre, Emeritus Universität Duisburg-Essen
Erstsendung: Januar 2018
© 2018 mce mediacomeurope GmbH
Sämtliche Sendungen von HYPERRAUM.TV sind nur für die persönliche Information bestimmt und sind urheberrechtlich geschützt. Kopieren, Vervielfältigung, Bearbeitung, Verbreitung und jede Art der Verwertung außerhalb der Grenzen des Urheberrechtes sind nicht gestattet. Downloads und Kopien dieser Seite sind für den kommerziellen Gebrauch nicht gestattet.
Bio, Chemie & Medizin Komplexitäts- & Systemforschung
TagsAntibiotika Antibiotikum Bakteriologie Binghamton Center for Biofilm Research Biochemie Biofilm Biofilm Centre EPS extrazelluläre polymere Substanz Genetik Genexpression Hans-Curt Flemming Hemholtz-Zentrum für Infektionsforschung Janne Thöming Karin Sauer Matrix Medizin Mikrobiologie Molekularbiologie Toleranzverhalten Twincore Universität Düsseldorf-Essen
No Comments